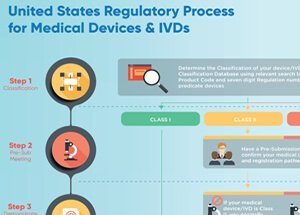
의료기기 FDA 인증
의료기기는 식품의약국(FDA)에 의해 규제됩니다. 특정 의료 기기는 FDA 승인을 받아야 판매됩니다. 코스미레그는 의료기기 미국 수출, FDA 의료기기 등록/승인, FDA 510(k), 시판전 허가 (PMA), FDA HDE, FDA IDE, FDA 드 노보 서비스를 지원합니다.
- 정확한 라벨 검토
- 빠른 처리
- 10+ 년의 경험
의료기기 FDA 인증 서비스
의료기기 등록
모든 의료기기 업체는 FDA에 의료기기 등록을 해야 합니다. 의료기기 업체는 FDA와 중개자 역할을 할 수 있는 미국 대리인을 지정해야 합니다. 코스미레그는 의료기기 FDA 등록을 위한 지원을 합니다.

시판 전 신고 FDA 510(k)
FDA 510(k)는 시판 전 신고로 해당기기가 법적으로 이미 시판되고 있는 기기와 동질성을 가졌다는 것을 증명하는 과정으로 코스미레그는 FDA 510(k) 인증을 도와드립니다.

시판전 허가(PMA)
고위험 장치(클래스 III)의 경우 시판전 허가(PMA)가 필요합니다. 의료기기의 안정성과 효율성을 과학적 근거를 통해 승인 받는 절차로 서류 심사와 제조시설 심사, 임상시험 실시에 대한 적합성 등 세밀한 확인 절차가 진행되며, 규정에 따른 임상연구와 효능에 대해 완벽한 보고자료를 작성해야 합니다. 시판전 허가(PMA)은 코스미레그와 상담하세요.

FDA HDE (인도적 기기 면제)
희귀 질환을 가진 환자의 치료 또는 관리에 사용되는 의료기기의 경우 시판전 허가(PMA)이 어려울 수 있는데 이 때 FDA HDE (인도적 기기 면제)를 통해 고위험 3등급 의료기기를 승인받게 됩니다. 코스미레스에서 FDA HDE 관련 컨설팅을 받아보세요
FDA IDE (의료기기 임상시험 승인 면제)
시판전 허가(PMA)를 충족하려면 의료기기 임상시험을 수행해야 합니다. 이 때 FDA IDE (의료기기 임상시험 승인 면제)를 통해 의료기기 사용과 판매에 특별 권한을 가질 수 있습니다. FDA IDE 신청은 코스미레그와 상의하세요.

FDA 드 노보
의료기기에 중대한 위험은 없으나 비교할 만한 동등의료기기가 없는 경우 3등급으로 분류됩니다. 이 때 FDA 드 노보 신청(513[g])을 통해 의료기기를 평가하게 됩니다. FDA 드 노보 신청, 코스미레그와 상의하세요.
무엇을 골라야할지 모르십니까?
무료 상담을 원하시면 지금 연락하십시오.
자주 묻는 질문:
의료기기의 위험도에 따라 세 가지 클래스 I (저위험), 클래스 II, 또는 클래스 III (고위험)로 기기를 분류됩니다. 고위험 기기에 해당하는 클래스 III의 경우 FDA 승인이 필요하며, 의료기기 업체는 안전성과 효과성을 입증해야 합니다.
클래스 I (저위험), 클래스 II 의료기기의 경우 FDA 승인이 필요하지 않습니다. 대신 FDA 시판 전 허가 510(k)를 제출해야 합니다. 이는 해당 의료기기가 법적으로 이미 시판되고 있는 기기와 동질성을 가졌다는 것을 증명하는 과정이며, FDA 510(k) 통과시 미국에서 판매할 수 있습니다.